17日凌晨,中国科学院广州生物医药与健康研究院联合华南理工大学、广州实验室、西湖大学的科研团队,在国际顶级学术期刊《细胞》上发表了突破性研究成果。
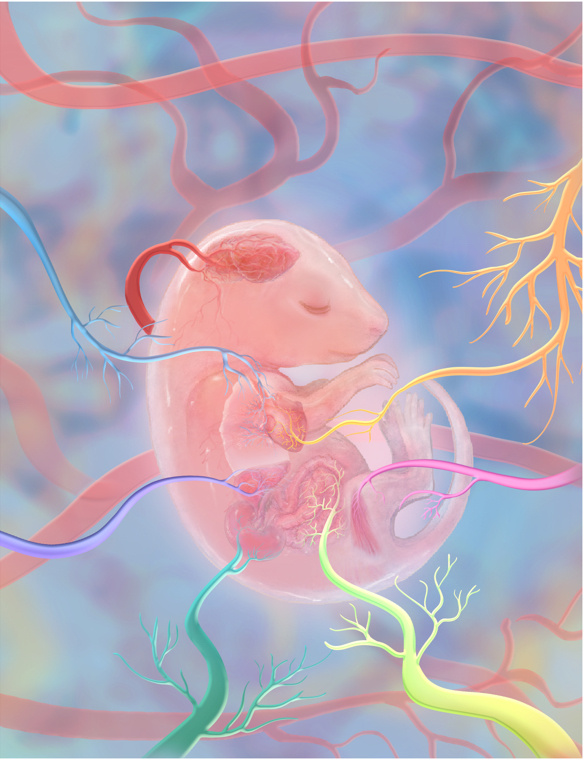
他们成功绘制出全球首个覆盖小鼠胚胎完整发育过程的内皮细胞“时空地图”,首次系统性揭示,在生命孕育的早期,遍布全身的血管内皮细胞就已开始学习各自器官的“语言”,分化出心、脑、肺、肝等器官特有的“定制化”血管。这项研究为理解心梗、脑梗等心脑血管疾病的器官特异性,以及未来在体外对血管开展工程化改造,奠定了全新的理论基础。
血管如同人体内遍布的“水路系统”,负责输送养分和氧气。构成血管内壁的内皮细胞,曾被认为是功能相似的“通用零件”。过去的研究主要关注同一器官内动脉与静脉的差异。然而,不同器官的血管是否从一开始就不同?却一直是未解之谜。
为此,研究团队“拍摄”了一部胚胎血管发育的“高清记录电影”,以半天为间隔,分析了小鼠从胚胎第7天到出生前共26个时间点、8个主要器官的内皮细胞。发现了三个层级的重要规律。





规律一是,研究发现,胚胎发育中期(约E9.0-E13.5)是血管“分道扬镳”的关键时间窗口。原本相同的血管内皮前体细胞,像接受了不同“岗位培训”,先后开始向心脏、大脑、肺、肝脏等器官的特有类型分化,并表达与器官功能紧密相关的独特基因和信号通路。
规律二是,揭示“人鼠殊途”的发育模式:跨物种对比发现,虽然人和小鼠的肺血管发育“路径图”和关键时间点相似,但高达70%的基因活动“节奏”完全不同。这提示,直接研究人类自身的发育规律至关重要,不能完全依赖小鼠模型进行简单推演。
规律三是,锁定肺血管“总工程师”——Casz1基因:研究以肺部血管为范本进行深度解密。发现一个名为 Casz1的基因,在人和小鼠的肺血管内皮中均特异性高表达,是调控肺血管网络精细构建的“关键开关”。当在血管内皮细胞中敲除Casz1后,小鼠肺血管生长受阻,无法形成关键的呼吸毛细血管,肺上皮细胞的发育也出现缺陷。机制上,Casz1如同一位“总工程师”,直接结合DNA,指挥一批与血管新生、肺特异性分化相关的基因协同工作。
论文作者、中国科学院广州生物医药与健康研究院研究员陈奇告诉记者,此次研究将为接下来人类细胞谱系设施的研究工作,提供理论和技术的重要积淀。人体由几十万亿细胞组成,这些细胞从一个受精卵开始,历经增殖、分化直至衰老的全生命周期动态演化过程,就是“细胞谱系”,解析细胞谱系,就是绘制细胞命运转变的高精度“导航图”。“这次研究,我们先绘制出小鼠细胞的‘导航图’,这将为接下来我们做人体的细胞谱系研究提供重要的支持。”陈奇说。

陈奇表示,这项看似基础的研究,未来将有很多应用前景。“为什么一些人容易患心肌梗死、脑梗死?这项研究为理解心脑血管疾病的特殊性、开发器官特异性治疗策略提供了‘分子地图’,为接下来的研究提供了新方向。”
本次研究还有望助力器官再生与药物研发,研究揭示了各器官血管与周围组织(如肺上皮)沟通的特定信号(如肺血管分泌的FGF1)。这些发现可为肺、肝等器官的损伤修复与再生提供新的干预靶点。
文/广州日报新花城记者:武威 通讯员:胡冰鑫
绘图:牛丽洁
广州日报新花城编辑:马俊贤






